杨业发医生的科普号
- 肝动脉灌注化疗(HAIC)与传统TACE(C-TACE)及载药微球栓塞(D-TACE)的比较
众所周知,肝动脉灌注化疗(HAIC)并不是一种最新的肝癌治疗技术。其实,早在二十世纪70年代就已经开始。当时主要通过外科肝动脉置管或血管内介入技术,进行肝动脉插管完成化疗药物的灌注。 为什么要将化疗药物放到肝动脉里呢?其实,这与肝脏的特殊的血管解剖结构有关,肝脏是具有双重血供的特殊器官,正常肝脏肝动脉血供约占1/4、门静脉血供约占3/4,而肝癌组织的血供几乎全部(约90%)由肝动脉提供,而门静脉供血则极少(约10%)。 从理论上,HAIC是通过肝动脉对肿瘤持续灌注高浓度细胞毒性药物,发挥最大限度的杀伤作用,而不会对正常肝脏组织造成大的不良影响。与全身化疗相比,在肝动脉里灌注化疗药物能够增加肿瘤组织局部药物的浓度,同时减少化疗药物在其他器官的分布,从而产生较强的抗肿瘤作用且降低全身副反应。 作为不可切除肝细胞癌(HCC)的一种治疗选择,经导管肝动脉化疗栓塞(Transcatheterarterialchemoembolization,TACE)自1978年由日本大阪市立大学医学部的山田(Yamada)教授提出以来,从此之后,TACE得到了非常广泛的运用,并显示出良好疗效。 近年来新型武器“药物洗脱微球”又称“载药微球”的出现进一步提高了TACE在部分患者身上的疗效。“载药微球”是一种能够吸附、携带化疗药物的新型栓塞物质(图1、图2),它在体内不可降解,进入肿瘤血管后一方面可以长久栓塞肿瘤血管,另一方面可以使化疗药物长时间作用于肿瘤内部,两种效果叠加,可以达到更好的局部控制效果。使用载药微球行肝动脉栓塞治疗称为D-TACE(Drug-elutingBead-TACE)。 HAIC的适应症1、伴有门静脉癌栓的肝癌患者,特别适合存在肝动脉-门静脉瘘,或者接受传统介入治疗但疗效不佳的肝癌患者。2、结直肠癌肝转移的患者。无法切除的结直肠肝转移病灶,采用HAIC治疗,病灶局部药物浓度可达外周静脉化疗的数十倍,具有肿瘤局部控制率高,全身副反应小等优势。过去常规的肝动脉灌注化疗采用顺铂方案,但研究表明以顺铂为基础的化疗方案疗效并不理想。目前,无论是对于原发性肝癌还是结直肠癌肝转移的患者,都主要采用以奥沙利铂为基础的FOLFOX方案(奥沙利铂,氟尿嘧啶,亚叶酸钙)。FOLFOX方案是晚期肝癌和结直肠癌获批的全身化疗方案,在晚期肝癌和结直肠癌患者中都展示出生存获益。HAIC和C-TACE和D-TACE有什么区别?与传统介入相比,肝动脉化疗灌注的化疗药物剂量大得多,尤其是氟尿嘧啶,剂量是传统介入的三倍多。外周血药物浓度的比较,HAIC>C-TACE>D-TACE(图3)。在给药时间上,传统介入(TACE)是短时间在肝动脉里注射化疗药物,D-TACE术后,载药微球可以在术后一个月的时间内缓慢释放加载的化疗药。而HAIC是持续的滴注化疗药物,达48小时。传统介入治疗及D-TACE基本为1-2个月/疗程,而肝动脉灌注化疗采用3周/疗程的方案,从最大程度地发挥化疗的作用。肝动脉灌注化疗术后有哪些不良反应?肝动脉灌注可能存在导管相关并发症,包括穿刺时动脉损伤,胃或十二指肠误灌注,脱管、堵管等,可通过调整导管位置,妥善固定导管,加强导管肝素化避免。HAIC治疗后患者发热的比例较C-TACE及D-TACE明显降低!HAIC治疗一般不使用颗粒栓塞剂,术中及术后发生异位栓塞的可能性非常低! 较大剂量的化疗药物的加入,肝动脉化疗灌注后容易出现骨髓抑制,表现为白细胞及血小板下降,化疗后可注射集落细胞刺激因子改善骨髓造血功能。另外,奥沙利铂容易引起外周神经炎,可口服营养神经药物缓解。
 徐伟 副主任医师 海军军医大学第三附属医院 放射介入科6866人已读
徐伟 副主任医师 海军军医大学第三附属医院 放射介入科6866人已读 - 胆管癌术后梗阻性黄疸伴胆道感染的介入微创治疗
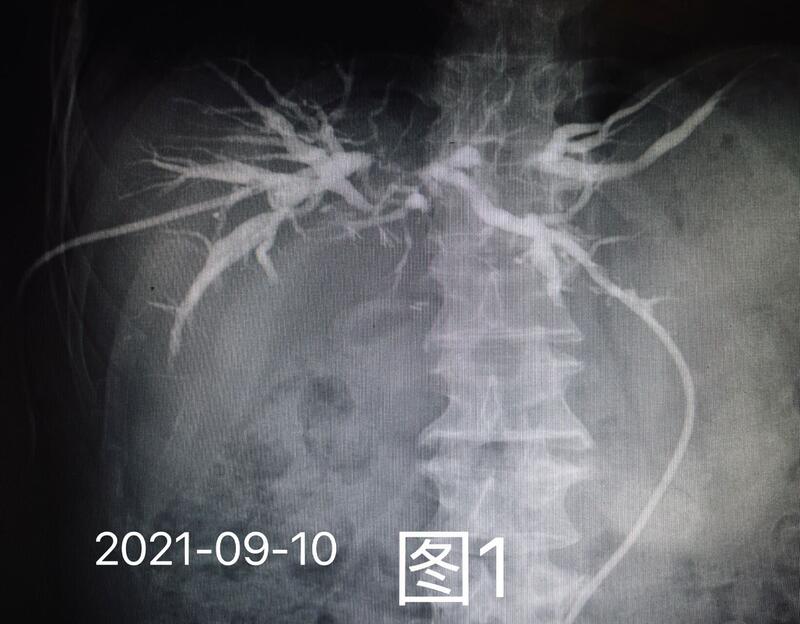
胆管癌是指源于肝外胆管包括肝门区至胆总管下端的胆管的恶性肿瘤。其病因可能与胆管结石、原发性硬化性胆管炎等疾病有关。临床可采用手术治疗、放射治疗、化学治疗等方法,但预后较差。梗阻性的黄疸,是由于各种原因引起的胆汁排泄障碍,从而引起胆汁在肝内淤积的一种病变。恶性梗阻性黄疸,通常是由于肝脏或者胆道系统的恶性肿瘤所引起。它的介入治疗方法,包括经皮肝穿刺胆道引流术以及胆道支架植入术。通过X线透视或超声引导,进行经皮向肝内胆道系统穿刺,通常选择右侧腋中线和剑突下入路。如果胆道梗阻严重,导管不能够通过狭窄段,就采用外引流。如果导管能够通过狭窄段,可以采用内外引流,胆汁部分引出体外,部分引入十二指肠。如果经过外引流或内外引流后,患者全身状况改善,经济条件允许,引流路径合适,可以放置胆道内支架进行引流!【经典病例】男性,55岁,胆管癌术后梗阻性黄疸,2021年9月放置双侧PTCD引流管(图1),2022年1月起反复发热,诊断为:胆道感染。2月16日更换双侧PTCD引流管(图2),术后胆红素不降反升,发热没有缓解。2月19日左侧放置第三根PTCD引流管,每日发热症状仍无缓解。2月24日患者在我科行胆道支架置入术(图3),术后发热很快消失,胆红素明显下降(图4)。
 徐伟 副主任医师 海军军医大学第三附属医院 放射介入科1361人已读
徐伟 副主任医师 海军军医大学第三附属医院 放射介入科1361人已读 - 什么是肝活检?
肝穿刺活检自1883年由德国医师开始最先开始在临床使用,至今已有130多年的历史。肝穿刺活体组织检查术(Liverbiopsy)简称肝活检,是采取肝组织标本的一种简易手段(图1)。由穿刺所得组织块进行组织学检查制成涂片做细胞学检查,经过处理后作病理组织学、免疫组化等染色,在显微镜下观察肝脏组织和细胞形态。现在肝穿刺最常用的方法是超声引导下经皮肝穿刺活检,但有凝血功能障碍及腹水者不适合,这类患者可选择经颈静脉肝活检。在检查过程中,通常只需要进行局部麻醉。超声引导下可直视患者的肝脏部位,有效避开重要血管和其他脏器并准确定位病灶。超声定位后的整个穿刺过程只需要几分钟。肝组织活检的穿刺方法有多种,如一般肝穿刺术、套管针穿刺术、分叶针切取术、快速肝穿刺术等。这些方法各有优缺点,前三种较易造成肝损伤或出血;后者属抽吸式活检针,较安全,多为临床所采用。肝病患者经过病史询问和体格检查,或者在辅以必要实验室和影像学检查,就可确诊。临床诊断疾病往往有一定的偏差,只有病理诊断才更确实可靠。有些不能通过以上检查明确诊断疾病,只有通过肝穿刺活检,进行病理学检查才能准确下结论,为后续的精准治疗提供依据。肝穿刺病理学检查主要用于各种肝脏疾病的鉴别诊断,如鉴别黄疸的性质和产生的原因,了解肝脏病变的程度和活动性,提供各型病毒性肝炎的病原学诊断依据,发现早期、静止期或尚在代偿期的肝硬化,判别临床疗效,尤其在确定肝纤维化严重程度上是国际公认的“金标准”。有些疾病诊断起来有困难,需要肝活检与临床症状相结合,才能作出诊断,如自身免疫性肝炎、慢性肝炎、原发性胆汁肝硬化及肝脏肿瘤等。肝穿刺有无危险,这是许多患者所关心和怀疑的一个问题。任何操作都有风险,肝穿刺也不例外,可能穿刺失败或发生疼痛、出血、恶性肿瘤针道转移等并发症。肝穿刺后出血的发生率在十万分之一左右,由于肝活检技术已经很成熟,只要掌握好适应症、禁忌症,在肝穿刺前做好充分的准备,肝穿刺活检的操作可做到万无一失。近年来多采用Menshini法一秒钟肝穿刺,少数患者于肝穿后除育穿刺点轻微疼痛及肩痛外无任何不适亦不遗留其它并发症。肝穿刺均是很成熟的技术。肝穿刺活检时取的肝组织很少,约为直径1mm、不到20mm长的一小条,约相当于肝脏的五百万分之一。肝穿刺是在超声引导下进行的,可以可避开大的血管等,相对来说是非常安全的。肝穿刺后建议卧床休息24小时,术后4小时内每隔15-30分钟测脉搏、血压一次,出现脉搏增快细弱、烦躁不安、血压下降、面色苍白、出冷汗以及内出血现象时,应赶快进行紧急处理,谨防大出血导致失血性休克等严重并发症。并发症的发生与肝穿前的准备,穿刺后的护理皆有关。因此,必须严密作好肝穿前的各项检查工作,严防肝穿后并发症的发生应列为首要。哪些患者需要做肝穿刺?1.原因不明的肝脾肿大或肝功能异常;2.原因不明的黄疸且已排除肝外胆道梗阻者;3.慢性肝炎随访病情或判断疗效,特别是对于乙肝的患者,肝组织病理是判断是否需抗病毒治疗的重要依据;4.疑有弥漫性肝病或肝外疾病累及肝脏者。5.观察治疗效果及判断预后:观察药物治疗后的病理改变情况,以进一步确定其疗效。也可根据肝脏病理改变判断患者的预后。6.确定肿瘤的来源:通过肝穿刺来判断肝癌是原发的还是继发的;是肝细胞性还是胆管细胞性。结合肿瘤基因检测等检查有助于评估是否用药敏感,可以更有效地实现对患者的“个体化”治疗。7.肝移植术后肝功能的评估等。哪些患者不适合做肝穿刺?⒈用临床常规检查方法已可达到目的者。2.有出血倾向的患者。如血友病、海绵状肝血管病、凝血时间延长、血小板减少达80×10的9次方/L以下者。⒊大量腹水或重度黄疸者。⒋严重贫血或一般情况差者。⒌肝昏迷者。⒍严重肝外阻塞性黄疸伴胆囊肿大者。⒎疑为肝包虫病或肝血管瘤者。8.严重心、肺、肾疾病或其功能衰竭者。9.9.右侧脓胸、膈下脓肿、胸腔积液或其他脏器有急性疾患者,穿刺处局部感染者。10.10.严重高血压(收缩压>24KPa)者。11.不能配合的病者。
 徐伟 副主任医师 海军军医大学第三附属医院 放射介入科932人已读
徐伟 副主任医师 海军军医大学第三附属医院 放射介入科932人已读 - 什么是门静脉栓塞(PVE)?
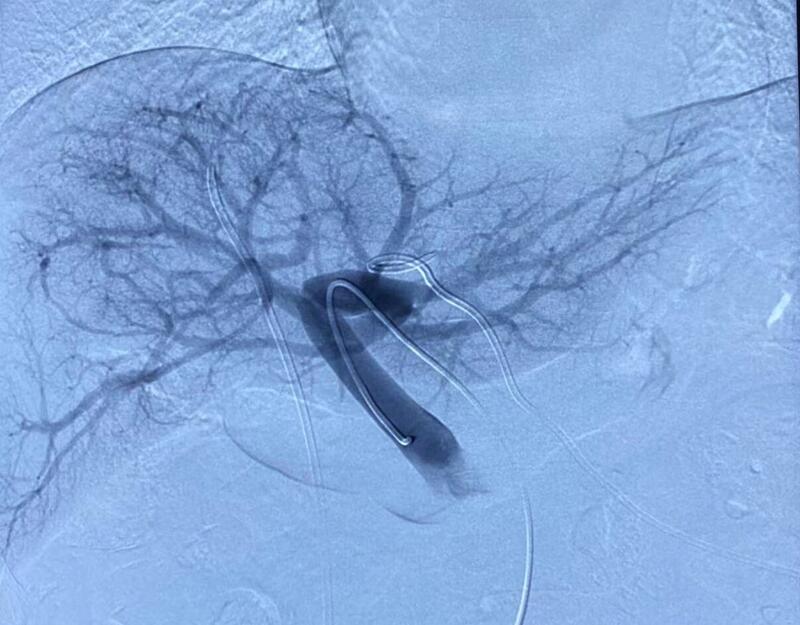
随着肝胆外科手术设备的不断进步及外科手术技巧的提高,行肝部分切除患者的围手术期越来越安全。而扩大肝切除的患者仍然具有较高的并发症发生率,患者恢复缓慢,风险较大。尤其对于巨块型肝癌及肝门部胆管癌,根治术后往往剩余的肝偏小,发生肝功能衰竭的风险较高,甚至可能会导致患者死亡。日本的幕内雅敏(Makuuchi)教授是现代肝脏外科的发展史上享誉世界的肝脏外科手术医生。1984年幕内雅敏(Makuuchi)教授首次将门静脉栓塞(Portalveinembolization,PVE)用于肝门胆管癌以来,在日本和欧美已被应用于转移性肝癌、肝细胞癌和胆道肿瘤。美国的麦道夫教授是世界著名门静脉栓塞术式(PVE)专家,来自世界首屈一指的癌症科研与治疗中心——MDAnderson癌症中心,他改进并发明了新的门静脉栓塞术式,使其风险大幅降低,成功率大幅提高。麦道夫教授在世界范围内累计门静脉栓塞总量第一,他领导的团队所行门静脉栓塞术后肝癌切除手术率高达92%,其结果使得肝癌病人的手术率大幅提高了50%;并使得手术质量的多个方面获得改善。麦道夫教授指出在中国,肝癌术前门静脉栓塞术可使多达3-4万因肝量不足失去根治性手术治疗机会的肝癌病人得到手术治疗的机会,这等同于给与这些病人长期生存甚至完全治愈的机会。近年来,因PVE能有效诱导剩余肝体积(futureliverremnant,FLR)的体积増大和功能增强,PVE术广泛用于外科肝肿瘤的肝切除术前,以扩大手术适应证、减少术后肝功能衰竭、感染、出血的发生。PVE作为一种术前辅助性治庁可以使剩余肝体积增大,可增加肝门胆管癌,转移性肝癌和肝细胞癌手术切除的安全性。PVE是一种介入微创手术。PVE术的4个主要目的:1)扩大外科手术适应证;2)防止肿瘤沿门静脉播散;3)防止门静脉瘤栓形成;4)配合动脉灌注使肿瘤完全坏死;哪些患者可行PVE?2010年肝癌治疗准则会议(AHPBA/SSAT)建议肝功能正常者,FLR<20%;合并脂肪肝、接受化疗患者FLR<30%;代偿性肝硬化,FLR<40%可考虑PVE。PVE的原理:1、血流增加。门静脉栓塞后,门静脉血流重新分布,完全流入未栓寒侧,文献报道未栓塞侧门静脉血流速度明显增快,后逐渐减慢,术后14d流速仍显著高于基线,且肝脏增生速度与血流流速呈正相关。2、促肝细胞生长物质由门脉提供。PVE术常用的常用的栓塞剂有α-氰基丙烯酸正丁酯胶((N-butyla-cyanoacrylate,NBCA)、明胶海绵、金属圈、PVA微粒等。2014年11月至2019年12月,海军军医大学第三附属医院共126例因FLR不足导致无法切除的肝细胞癌(HCC)或肝内胆管癌(ICC)病人,采用α-氰基丙烯酸正丁酯胶((N-butyla-cyanoacrylate,NBCA)、微球、明胶海绵作为栓塞材料的PVE组.最终结果显示,采用NBCA及微球作为栓塞材料的PVE导致FLR增长速率低于ALPPS,两种栓塞材料的PVE二期手术切除率相当.使用NBCA作为栓塞材料的PVE其FLR增长速率高于微球,且这两种栓塞材料的栓塞效果均优于明胶海绵.(肝门部胆管癌合并黄疸患者,行PTCD治疗后)PVE手术经过(图1-图3):局麻,在超声引导下,用18GEV针穿刺门静脉左侧分支,置入单弯导管,于门静脉主干内造影显示门静脉全貌(图1)。单弯导管超选至右侧门脉主干内,为了栓塞的更彻底,应尽量将微导管超选择性进入到门脉右侧分支的最末端,以NBCA胶进行彻底栓塞(图2),栓塞满意后,将单弯导管至于门静脉主干内复查造影,显示栓塞良好(图3)。栓塞结束后,为了降低术后出血的风险和防止误栓塞左侧门静脉,我们将单弯导管头端回撤至肝实质内,手术后第二天分三次逐步拔除造影导管。除非门静脉受累或癌栓形成,临床上很少看到由于门静脉血流增加导致的增生,所以理论上患者均有进行扩大肝切除的可能,那么门静脉栓塞(PVE)就没有绝对的禁忌证。只有相对禁忌证:(1)残余肝、肝外脏器或门静脉周围淋巴结转移;(2)难以纠正的凝血障碍;(3)肿瘤累及到门静脉主干;(4)肝内多发转移灶;(5)存在门静脉血流增加导致的肝增生;门静脉栓塞(PVE)的术后并发症比较少见,主要有:肝包膜下出血、腹腔出血、胆道出血、假性动脉瘤、动静脉漏、动脉门静脉分流等。
 徐伟 副主任医师 海军军医大学第三附属医院 放射介入科2945人已读
徐伟 副主任医师 海军军医大学第三附属医院 放射介入科2945人已读





